
- Autors Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Pēdējoreiz modificēts 2025-01-22 17:04.
C8H18
Kāda ir oktāna c8h18 empīriskā formula?
The oktāna empīriskā formula $$C_{8}H_{18}$$ ir: A. B. C.
Līdzīgi, kāda ir c2h6o2 empīriskā formula? Molekulārās un empīriskās formulas
| Jautājums | Atbilde |
|---|---|
| Uzrakstiet empīrisko formulu šādam savienojumam: C6H8 | C3H4 |
| Uzrakstiet empīrisko formulu šādam savienojumam: X39Y13 | X3Y |
| Kāda ir savienojuma WO2 empīriskā formula? | WO2 |
| Uzrakstiet savienojuma C2H6O2 empīrisko formulu? | CH3O |
Ziniet arī, kā jūs atrodat empīrisko formulu?
Sāciet ar katra elementa gramu skaitu, kas norādīts uzdevumā. Pārvērtiet katra elementa masu molos, izmantojot molāro masu no periodiskās tabulas. Sadaliet katru molu vērtību ar mazāko aprēķināto molu skaitu.
Kas ir oktāna izomēri?
Oktānskaitlis ir 18 strukturālas izomēri (24, ieskaitot stereoizomērus): Oktānskaitlis (n- oktānskaitlis ) 2-metilheptāns. 3-metilheptāns (2 enantiomēri)
Ieteicams:
Kāpēc magnija oksīda empīriskā formula ir MgO?

Magnija oksīda empīriskā formula ir MgO. Magnijs ir +2 katjons, bet oksīds ir -2 anjons. Tā kā lādiņi ir vienādi un pretēji, šie divi joni savienosies atomu attiecībās 1 pret 1
Kāda ir kofeīna empīriskā formula?
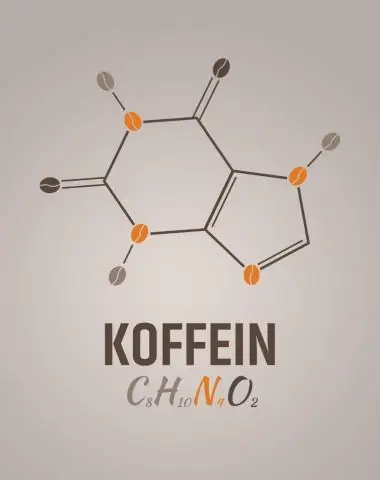
2 atbildes. C8H10N4O2 ir kofeīna molekulārā formula
Kāda ir stroncija bromīda empīriskā formula?

SrBr2 Kāda tad ir stroncija bromīda formula? SrBr2 Turklāt, vai stroncija bromīds ir ūdens? Par Stroncija bromīds Heksahidrāts Var apsvērt īpaši augstas tīrības, augstas tīrības, submikronu un nanopulvera formas. Lielākā daļa metāla bromīds savienojumi ir ūdenī šķīstoši.
Kas ir empīriskā formula un molekulārā formula?
Molekulārās formulas norāda, cik atomu katrā elementā ir savienojumā, un empīriskās formulas norāda vienkāršāko vai samazinātāko elementu attiecību savienojumā. Ja savienojuma molekulāro formulu vairs nevar reducēt, tad empīriskā formula ir tāda pati kā molekulārā formula
Kāda ir savienojuma empīriskā formula?

Savienojuma empīriskā formula ir katra savienojuma atoma veida vienkāršākā veselo skaitļu attiecība. Tā var būt tāda pati kā savienojuma molekulārā formula, bet ne vienmēr. Empīrisku formulu var aprēķināt no informācijas par katra elementa masu savienojumā vai no procentuālā sastāva
