
- Autors Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Pēdējoreiz modificēts 2025-01-22 17:04.
Kāpēc abas galvaniskās šūnas sastāvdaļas ir atdalītas viens no otra? Metāli ir novietoti pus- šūnas kuras savieno sāls tilts. Elektronu kustība no anoda uz katodu ir elektriskā strāva.
Kāpēc abas šūnas sastāvdaļas ir atdalītas viena no otras?
Galvanikā šūna tur ir divi pus- šūnas . Katrs pus- šūna satur elektrodu elektrolītā. The atdalīšana ir nepieciešams, lai novērstu oksidācijas un reducēšanas reakciju tiešu ķīmisko kontaktu, radot potenciālu atšķirību.
Zināt arī, kam tiek izmantoti galvaniskie elementi? Galvaniskās šūnas . Starp citiem šūnas , a galvaniskais šūna ir veids elektroķīmiski šūna. Tas ir lietots nodrošināt elektrisko strāvu, veicot elektronu pārnesi caur redoksreakciju. A galvaniskais šūna ir priekšstats par to, kā enerģiju var izmantot, izmantojot vienkāršas reakcijas starp dažiem dotajiem elementiem.
Tātad, kāpēc elektroķīmiskajā šūnā ir 2 pusšūnas?
Elektroķīmiskās šūnas parasti sastāv no divas pusītes - šūnas . Puse - šūnas atsevišķi uz oksidēšanās puse -reakcija no uz samazināšana puse -reakciju un ļauj strāvai plūst caur ārējo vadu. Samazinājums notiek plkst uz katods. Sāls tilta pievienošana ir pabeigta uz ķēde, kas ļauj plūst strāvai.
Kādi ir divu veidu elektroķīmiski elementi?
Divi veidi no Šūna Tur ir divi fundamentāli elektroķīmisko elementu veidi : galvaniskais un elektrolītiski. Galvaniskās šūnas pārveidot ķīmisko potenciālo enerģiju elektroenerģijā. Enerģijas pārveide tiek panākta ar spontānām (ΔG < 0) redoksreakcijām, kas rada elektronu plūsmu.
Ieteicams:
Kā augu šūnas forma atšķiras no dzīvnieku šūnas formas?
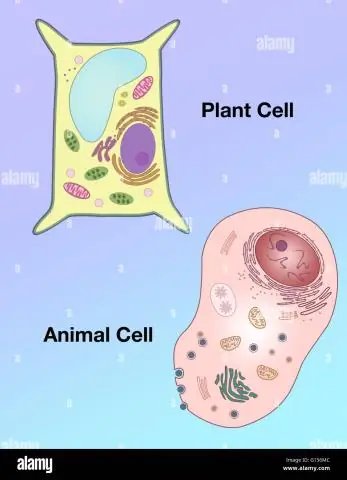
Vakuoli: augu šūnām ir liela vakuola, savukārt dzīvnieku šūnās ir vairāki mazi vakuoli. Forma: augu šūnām ir regulārāka forma (parasti taisnstūrveida), bet dzīvnieku šūnām ir neregulāras formas. Lizosomas: parasti atrodas dzīvnieku šūnās, savukārt augu šūnās to nav
Kādas ir elektroķīmiskās šūnas sastāvdaļas?

A) Elektroķīmisko elementu elektroda sastāvdaļas: tas ir ciets elektrības vadītājs, kas izgatavots no metāla (dažreiz nemetāla, piemēram, grafīta). Šūna sastāv no diviem elektrodiem. Vienu sauc par anodu, bet otru sauc par katodu. Elektrolīts: to veido jonu vai kausētu sāļu šķīdumi, kas var vadīt elektrību
Kāpēc prokariotu šūnas ir mazākas nekā eikariotu šūnas?
Atbilde un skaidrojums: Prokariotu šūnas mēdz būt mazākas, jo tajās ir daudz mazāk. Eikariotu šūnām ir vairākas ar membrānām saistītas organellas, piemēram, a
Kā sauc simbiotiskas attiecības, kurās ieguvējas abas sugas?

Mutuālisms ir simbiotiskas attiecības, kurās gūst labumu abas sugas. Kommensālisms ir simbiotiskas attiecības, kurās viena suga gūst labumu, bet cita suga netiek ietekmēta. Parazītisms ir simbiotiskas attiecības, kurās viena suga (parazīts) gūst labumu, bet otra suga (saimnieks) tiek nodarīts kaitējums
Kādas DNS abas puses satur kopā?

Slāpekļa bāzes abās DNS virknēs savienojas pārī, purīns ar pirimidīnu (A ar T, G ar C), un tos satur vājas ūdeņraža saites. Vatsons un Kriks atklāja, ka DNS ir divas puses jeb dzīslas un ka šīs dzīslas ir savītas kopā kā savītas kāpnes - dubultā spirāle
