
- Autors Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Pēdējoreiz modificēts 2025-01-22 17:05.
Tātad jebkura elektronu konfigurācija kurā uz Pēdējais elektrons (atkal, uz valence elektrons ) ir iekšā a augstākas enerģijas orbitāle, šis elements tiek uzskatīts par an satraukts stāvoklis . Piemēram, ja mēs skatāmies pamatstāvoklis ( elektroni iekšā uz enerģētiski zemākā pieejamā skābekļa orbitāle, elektronu konfigurācija ir 1s22s22p4.
Ziniet arī, ko tas nozīmē ar pamata stāvokļa elektronu konfigurāciju?
The pamata stāvokļa elektronu konfigurācija ir izkārtojums elektroni ap atoma kodolu ar zemāku enerģijas līmeni. The elektroni aizņemot dažādu enerģijas līmeņu orbitāles, dabiski krīt uz zemāko enerģiju Valsts vai zemes stāvoklis.
Papildus iepriekš minētajam, kāda ir Mn atoma elektronu konfigurācija pamatstāvoklī? The pamata stāvokļa elektronu konfigurācija no zemes stāvoklis gāzveida neitrāls mangāns ir [Ar]. 3d5. 4s2 un termins simbols ir 6S5/2.
Kurš no tiem ir pamata stāvokļa konfigurācijā?
A zeme - Valsts atoms ir atoms, kurā elektronu kopējo enerģiju nevar pazemināt pārnesot viens vai vairāk elektronu uz dažādām orbitālēm. Tas ir, a zeme - Valsts atoms, visi elektroni atrodas iespējami zemākajos enerģijas līmeņos. piem.: Apsveriet oglekļa atomu, kura elektronu konfigurācija ir sekojošs.
Kas ir Hunda likums?
Hunda noteikums . Hunda likums : katra orbitāle apakšapvalkā ir atsevišķi aizņemta ar vienu elektronu, pirms jebkura orbitāle ir divreiz aizņemta, un visiem atsevišķi aizņemtām orbitālēm elektroniem ir vienāds spins.
Ieteicams:
Kāda ir hlora elektronu konfigurācija ierosinātā stāvoklī?

Kura elektronu konfigurācija attēlo hlora atomu ierosinātā stāvoklī? (2) 2-8-6-1 tas ir hlora ierosinātais stāvoklis, periodiskajā tabulā pamatstāvoklis ir 2-8-7. Ierosinātā stāvokļa elektronu konfigurācija parāda, ka elektrons atstāj vienu enerģijas līmeni un virzās uz augstāku līmeni
Kāda ir slāpekļa galvenā valences elektronu konfigurācija?
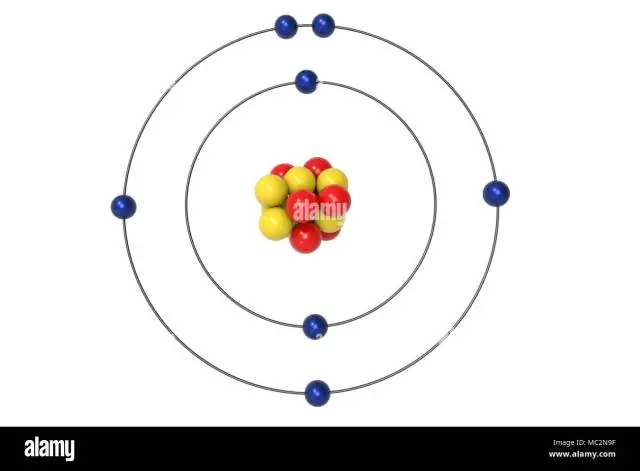
Atlikušie trīs elektroni dosies 2p orbitālē. Tāpēc N elektronu konfigurācija būs 1s22s22p3. Slāpekļa (N) konfigurācijas apzīmējums nodrošina vienkāršu veidu, kā zinātnieki var rakstīt un sazināties, kā elektroni ir izvietoti ap slāpekļa atoma kodolu
Cik 3D elektronu atrodas hroma atoma pamatstāvoklī?

Hroma atomos ir 24 elektroni, un apvalka struktūra ir 2,8. 13.1. Pamatstāvokļa gāzveida neitrāla hroma elektronu konfigurācija ir [Ar]. 3d5
Kura ir bora viktorīnas elektronu konfigurācija?

Bora elektronu konfigurācija ir 1s (2) 2s (2) 2p (1)
Kas notiek, kad elektroni atgriežas savā pamatstāvoklī?

Atoms pāriet no pamatstāvokļa uz ierosinātu stāvokli, uzņemot enerģiju no apkārtējās vides procesā, ko sauc par absorbciju. Elektrons absorbē enerģiju un pāriet uz augstāku enerģijas līmeni. Apgrieztā procesā, emisijā, elektrons atgriežas pamatstāvoklī, atbrīvojot papildu enerģiju, ko tas absorbējis
