
- Autors Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Pēdējoreiz modificēts 2025-01-22 17:05.
Šīs mijiedarbības ir iespējamas, salokoties līdz olbaltumvielu ķēdei, lai tuvinātu attālās aminoskābes. 2. Terciāro struktūru stabilizē disulfīda saites, jonu mijiedarbība, ūdeņraža saites , metāliskās saites un hidrofobās mijiedarbības.
Tikai tā, kādas mijiedarbības stabilizē proteīna terciāro struktūru?
Galvenais spēks, kas stabilizē terciāro struktūru, ir hidrofobā mijiedarbība starp nepolārajām sānu ķēdēm proteīna kodolā. Papildu stabilizējošie spēki ietver elektrostatisko mijiedarbību starp pretēja lādiņa jonu grupām, ūdeņraža saites starp polārajām grupām un disulfīds obligācijas.
Var arī jautāt, kura no šīm aminoskābēm ir iesaistīta kovalentajā saitē, kas stabilizē daudzu proteīnu terciāro struktūru? Tāpat kā ar disulfīda tiltiem, šie ūdeņraža saites var apvienot divas ķēdes daļas, kas atrodas zināmā attālumā secības ziņā. Sāls tilti, jonu mijiedarbība starp pozitīvi un negatīvi lādētām vietām aminoskābju sānu ķēdēs, arī palīdz stabilizēt proteīna terciāro struktūru.
Ņemot to vērā, kā aminoskābes ietekmē proteīna terciāro struktūru?
Reiz nepolārais aminoskābes ir izveidojuši nepolāro kodolu olbaltumvielas , vājie van der Vāla spēki stabilizē olbaltumvielas . Turklāt ūdeņraža saites un jonu mijiedarbība starp polārajām, lādētajām aminoskābes veicināt terciārā struktūra.
Kā tiek uzturēta proteīna terciārā struktūra?
Paskaidrojums: terciāro struktūru stabilizē vairākas mijiedarbības, īpaši sānu ķēdes funkcionālās grupas, kas ietver ūdeņraža saites , sāls tilti, kovalentie disulfīda saites un hidrofobās mijiedarbības.
Ieteicams:
Kurš atklāja DNS viktorīnas struktūru?
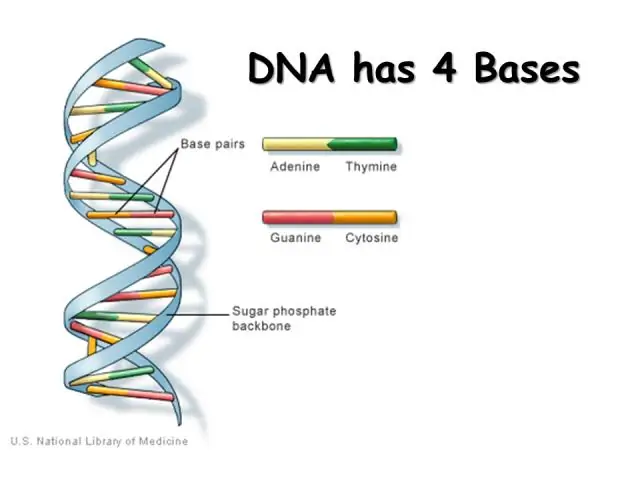
Zinātnieki atzīst DNS struktūras atklāšanu (publicēts 1953. gadā žurnālā Nature). Lai gan Vatsons un Kriks tika atzīti par atklājumu, viņi nebūtu zinājuši par šo struktūru, ja nebūtu redzējuši Rozalindas Franklinas un Morisa Vilkinsa pētījumus
Kāda veida saite stabilizē terciāro olbaltumvielu struktūru?

Olbaltumvielas terciārā struktūra attiecas uz tās polipeptīdu ķēdes kopējo trīsdimensiju izvietojumu telpā. To parasti stabilizē ārējās polārās hidrofilās ūdeņraža un jonu saišu mijiedarbības, kā arī iekšējās hidrofobās mijiedarbības starp nepolārajām aminoskābju sānu ķēdēm (4.-7. attēls)
Kāda aminoskābe ir C?

Aminoskābju kodi Ala A Alanīns Cys C Cisteīns Gln Q Glutamīns Glu E Glutamīnskābe Gly G Glicīns
Kāda ir saistība starp struktūru un funkciju viktorīnu?

Struktūras forma nosaka tās funkciju. Piemēram, ja proteīna forma mainās, tā vairs nespēj pildīt savas funkcijas. Olbaltumvielām, kas ir fermenti, ir ļoti specifiska forma, līdzīgi kā durvju atslēga
Kāda aminoskābe ir Agu?

Aminoskābju DNS bāzes trīskārši M-RNS kodoni serīns AGA, AGG, AGT, AGC TCA, TCG UCU, UCC, UCA, UCG AGU, AGC stop ATT, ATC, ACT UAA, UAG, UGA treonīns TGA, TGG, TGT, TGC ACU , ACC, ACA, ACG triptofāns ACC UGG
