
- Autors Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Pēdējoreiz modificēts 2025-01-22 17:05.
Izotopi ir dažādas atomu masas. Katra relatīvā pārpilnība izotopu var jānosaka, izmantojot masas spektrometrija . A masas spektrometrs jonizē atomus un molekulas ar augstas enerģijas elektronu staru un pēc tam novirza jonus caur magnētisko lauku, pamatojoties uz to masa -uzlādes attiecības (m/z m/z m/z).
Kā masu spektrometrijas dati parāda izotopu esamību?
Nē, lielākā daļa elementu pastāv dabā kā savādāks izotopi no tā paša elementa. Kad tīra elementa paraugs ir analizēts ar a masas spektrometrs , katrs izotopu būs tikt jonizētam un atklātam. The masa spektrs pārstāv katru izotops kā virsotne, uzzīmējot tās masa lādiņa (m/z) attiecība un tās relatīvā intensitāte.
Kā arī aprēķināt izotopa vidējo masu? Uz aprēķināt uz vidējā masa , vispirms konvertējiet procentus daļdaļās (daliet tos ar 100). Tad aprēķināt uz masa cipariem. Hloru izotops ar 18 neitroniem ir 0,7577 pārpilnība un a masa skaits 35 amu.
Attiecīgi, kā masu spektrometrija identificē savienojumus?
Augstākais- masa jonu a spektrs ir parasti tiek uzskatīts par molekulāro jonu, un zemāks masa joni ir fragmenti no molekulārā jona, pieņemot paraugu ir viens tīrs savienojums . Lai arī šie savienojumi ir ļoti līdzīga izmēra, tas ir vienkārša lieta identificēt tos no viņu indivīda masa spektri.
Kāda ir 1 amu masa?
Atomu masas vienība (simbolizēta AMU vai amu) ir definēta kā precīzi 1/12 no oglekļa-12 atoma masas. Oglekļa-12 (C-12) atomam ir seši protoni un seši neitroni savā kodolā. Neprecīzā izteiksmē viens AMU ir vidējais rādītājs protonu atpūtas masa un neitronu atpūtas masa.
Ieteicams:
Ko parāda broma tests?

Organiskajā ķīmijā broma tests ir kvalitatīvs tests nepiesātinājuma (oglekļa-oglekli dubultsaites vai trīskāršās saites) un fenolu klātbūtnei. Jo nepiesātinātāks ir nezināmais, jo vairāk broma tas reaģē, un jo mazāk krāsains būs šķīdums
Ko parāda viļņu frontes diagramma?

Viļņa frontes diagramma parāda, cik bieži ir redzama viļņa virsotne. Normālos apstākļos tā būs vienkārši diagramma ar līnijām, kas atrodas vienādā attālumā viena no otras, jo viļņu virsotnes atrodas konsekventos attālumos viena no otras
Kā kompass parāda virzienu?

Kompasus galvenokārt izmanto navigācijā, lai atrastu virzienu uz zemes. Tas darbojas, jo pašai Zemei ir magnētiskais lauks, kas ir līdzīgs stieņa magnēta laukam (skatiet attēlu zemāk). Kompasa adata sakrīt ar Zemes magnētiskā lauka virzienu un norāda ziemeļu-dienvidu virzienā
Ko grafiks parāda par zvaigznes krāsas un temperatūras saistību?
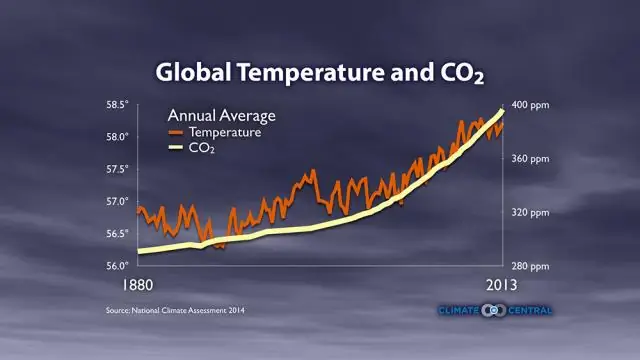
Sarkanākajām zvaigznēm temperatūra ir zemāka, bet zilākām zvaigznēm ir augstāka. B. Ko grafiks parāda par zvaigznes krāsas un temperatūras saistību? Jo tieša korelācija, jo zilāka zvaigzne, jo karstāka tā ir, jo sarkanāka zvaigzne, jo vēsāka tā ir
Kāda ir atšķirība starp protona masu un elektrona masu?
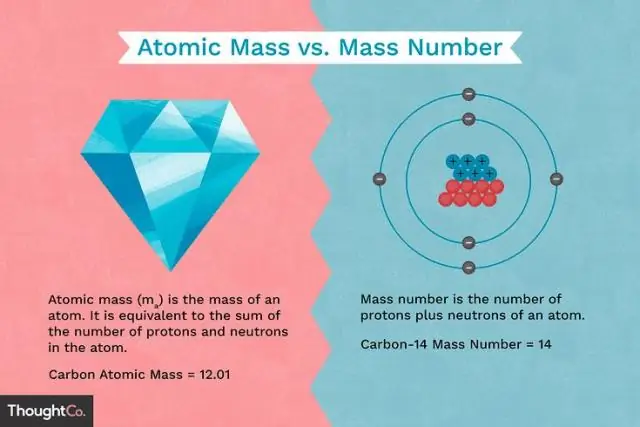
Protoniem un neitroniem ir aptuveni vienāda masa, taču tie abi ir daudz masīvāki par elektroniem (apmēram 2000 reižu masīvāki par elektronu). Protona pozitīvais lādiņš ir vienāds ar elektrona negatīvo lādiņu
