
Satura rādītājs:
- Autors Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Pēdējoreiz modificēts 2025-01-22 17:05.
Hendersona-Haselbalha vienādojuma atvasināšana
- Veikt vājas skābes (HA) jonizācijas reakciju:
- Iepriekš minētās reakcijas disociācijas konstante Ka būs:
- Pēc tam no vienādojums (2) izņemiet [H?] kreisajā pusē (atrisiniet H?):
- Aizstāt pH un pKa vienādojums (4):
Līdzīgi, kas ir Hendersona vienādojums ķīmijā?
Atjaunināts 2019. gada 10. augustā Hendersons Haselbalhs vienādojums ir aptuvens vienādojums kas parāda saistību starp šķīduma pH vai pOH un pKa vai pKb un disociēto vielu koncentrāciju attiecība ķīmiska sugas.
Tāpat, ko nozīmē pKa? Galvenās līdzņemamās lietas: pKa definīcija The pKa vērtība ir viena no izmantotajām metodēm norādīt skābes stiprums. pKa ir skābes disociācijas konstantes vai Ka vērtības negatīvais logs. A zemāka pKa vērtība norāda uz stiprāku skābi. Tas ir, zemākā vērtība norāda, ka skābe pilnīgāk disociējas ūdenī.
Ņemot to vērā, kāda ir pKa formula?
pKa ir definēts kā -log10 Ka kur Ka = [H+][A-] / [HA]. No šiem izteicieniem var atvasināt Hendersona-Haselbalha vienādojums kurš ir. pKa = pH + log [HA] / [A-] Tas norāda, ka tad, kad pH = pKa tad piesakieties [HA] / [A-] = 0, tāpēc [HA] = [A-], ti, vienādas summas no abām formām.
Vai ūdens ir buferis?
Ūdens ir buferis kaut arī nabadzīgs. Tas ir tāpēc, ka H20 pats jonizējas, veidojot H30+ un OH-. Lai veidotu skābi bufera buferis jums ir nepieciešama vāja skābe ar konjugētu bāzi. Tā kā būs hidronija un hidroksīda joni, jā, tas darbojas kā a buferis bet tas ir šausmīgs.
Ieteicams:
Kā pierādīt lielo skaitļu likumu?

VIDEO Ziniet arī, kā izskaidrot lielo skaitļu likumu? The lielo skaitļu likums norāda, ka novērotā parauga vidējais rādītājs no a liels izlase būs tuvu patiesajam populācijas vidējam rādītājam un tuvosies, jo lielāka būs izlase. Tāpat kāds ir lielo skaitļu vājais likums?
Kā pierādīt, ka taisnes ir paralēlas pierādījumos?

Pirmais ir, ja attiecīgie leņķi, leņķi, kas atrodas vienā stūrī katrā krustojumā, ir vienādi, tad līnijas ir paralēlas. Otrais ir, ja alternatīvie iekšējie leņķi, leņķi, kas atrodas šķērsenisko līniju pretējās pusēs un paralēlo līniju iekšpusē, ir vienādi, tad līnijas ir paralēlas
Kā pierādīt nepārtrauktību?

Definīcija: funkcija f ir nepārtraukta pie x0 savā domēnā, ja katram ϵ > 0 ir δ > 0 tā, ka ikreiz, kad x atrodas f un |x apgabalā &mīnus; x0| < δ, mums ir |f(x) &mīnus; f(x0)| < ϵ. Atkal mēs sakām, ka f ir nepārtraukts, ja tas ir nepārtraukts katrā savā domēna punktā
Kā pierādīt, ka kaut kas ir pamats?

VIDEO Jautāja arī, kas veido pamatu? Matemātikā elementu (vektoru) kopu B vektoru telpā V sauc par a pamata , ja katru V elementu var uzrakstīt unikālā veidā kā (galīgu) lineāru B elementu kombināciju. pamata tiek saukti pamata vektori.
Kā jūs varat pierādīt, ka 2 trijstūri ir līdzīgi, izmantojot sānu leņķa malas SAS līdzības postulātu?
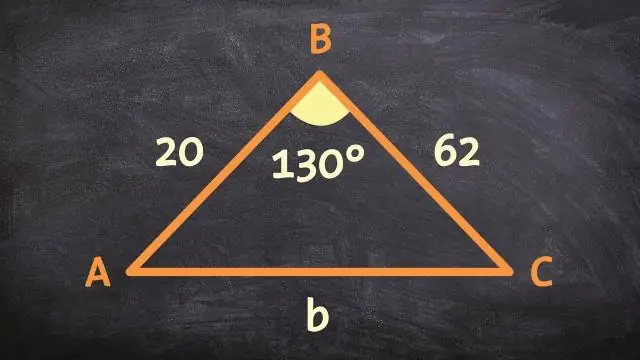
SAS līdzības teorēma nosaka, ka, ja viena trijstūra divas malas ir proporcionālas divām malām citā trijstūrī un abos ietvertais leņķis ir kongruents, tad abi trīsstūri ir līdzīgi. Līdzības transformācija ir viena vai vairākas stingras transformācijas, kam seko dilatācija
